Sulfonsäuren haben C–SO3H als funktionelle Gruppe wobei der Schwefel direkt an Kohlenstoff gebunden ist. Ihre Acidität ist wesentlich stärker als die der Carbonsäuren. Die Salze werden Sulfonate genannt. Die Monosulfonsäuren höherer Alkane dienen als Ausgangsmaterial für die Herstellung synthetischer Waschmittel. Zu den am meisten produzierten Detergenzien gehören die Alkylbenzolsulfonate mit einem Alkylrest, der 8 bis 14 Kohlenstoffatome enthält. Diese synthetischen Waschmittel haben gegenüber den Seifen den Vorteil, daß sie keine unlöslichen Calciumsalze bilden.
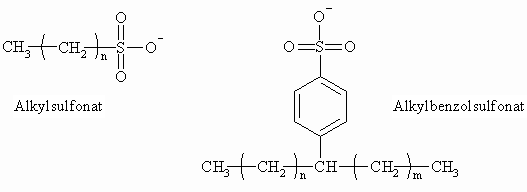
Wie bei den Carbonsäuren gibt es auch bei den Sulfonsäuren analoge Derivate wie z.B. Sulfonsäurehalogenide, -amide und –ester.
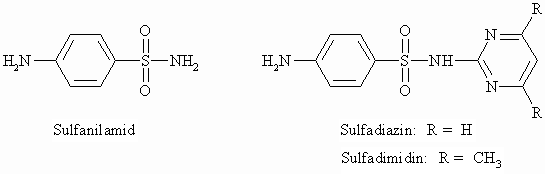
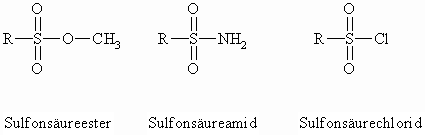
Am reaktivsten sind, wie bei den Derivaten der Carbonsäuren, die Sulfonsäurehalogenide. Sie reagieren mit Ammoniak oder Aminen zu den Sulfonsäureamiden. Diese besitzen vielfach pharmazeutische Bedeutung infolge ihrer bakteriziden Wirksamkeit. Sulfanilamid, besonders aber die sich davon ableitenden Sulfonamide, sind wirksame Chemotherapeutika gegen Bakterien-Infektionen. Im Bereich der Tiermedizin sind hier z.B. Sulfadiazin und Sulfadimidin zu nennen.
Als Beispiel aus dem Bereich der Humanmedizin sei noch das Sulfamethoxazol erwähnt.
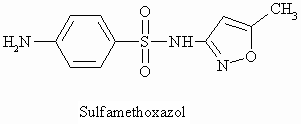
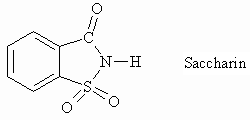
Auch der Süßstoff Saccharin ist ein Derivat einer Sulfonsäure; es ist ein gemischtes Imid aus einer Sulfon- und einer Carbonsäure.