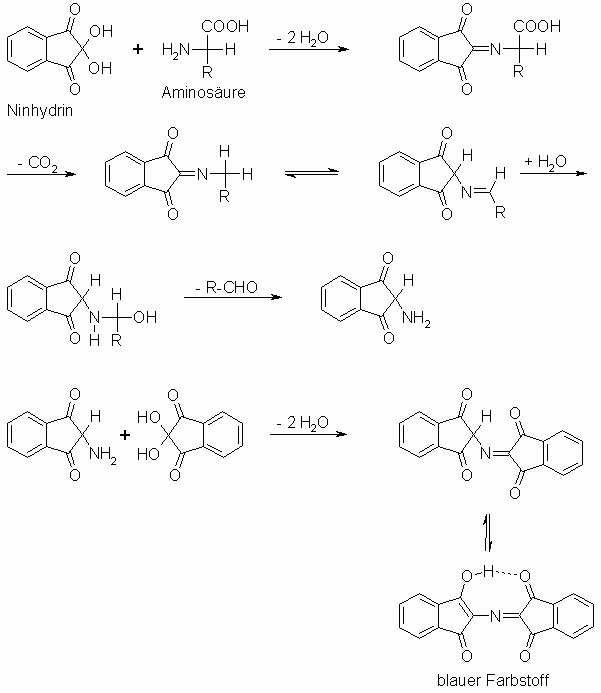
Neben den Hydroxycarbonsäuren stellen die Aminocarbonsäuren eine wichtige Stoffklasse dar. Besondere Bedeutung kommt den a -Aminocarbonsäuren (kurz: Aminosäuren) zu. Aus ihnen sind die Peptide und Proteine (siehe Kapitel XX) aufgebaut. Sie haben folgende, allgemeine Struktur:
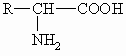
Außer wenn R gleich H ist (Glycin), haben alle Aminosäuren ein asymmetrisches a -Kohlenstoffatom und sind somit optisch aktiv.
Nomenklatur der Aminosäuren
| Typ | Name |
Formel |
Code1) | Funktion |
| Monoamino-monocarbonsäure | Glycin |
1 |
Gly/G | |
| dito | Alanin |
2 |
Ala/A | |
| dito | Serin |
3 |
Ser/S | |
| dito | Cystein |
4 |
Cys/C | |
| dito | Cystin |
5 |
Aufbau der Plasma-Eiweißstoffe, Entgiftung tox. Stoffwechselprodukte | |
| dito | Phenylalanin* |
6 |
Phe/F | Ausgangsstoff für die Bildung des Tyroxins, Adrenalins usw.; bei Fehlen Störungen der Schilddrüsen- und Nebennierenrinden-Funktion |
| dito | Tyrosin |
7 |
Tyr/Y | |
| dito | Threonin* |
8 |
Thr/T | Zur Verwertung der Aminosäuren der Nahrung |
| dito | Methionin* |
9 |
Met/M | Für das Wachstum des Körpers und der Haare. Leber-Schutzfunktion. Bei Fehlen Leberverfettung, Muskel-atrophie und Anämie |
| dito | Valin* |
10 |
Val/V | Notwendig zur normalen Funktion des Nervensystems. Bei Fehlen Hyperästhesie und Krämpfe |
| dito | Leucin* |
11 |
Leu/L |
Zum Aufbau der Plasma- und Gewebe-Eiweißkörper |
| dito | Isoleucin* |
12 |
Ile/I | Zur Verwertung der Aminosäuren der Nahrung. Fehlen bewirkt Gewichtsabnahme |
| Diamino-monocarbonsäure | Arginin* |
13 |
Arg/R | Für das Wachstum des Körpers |
| dito | Lysin* |
14 |
Lys/K | Für das Wachstum des Körpers. Bei Fehlen Zwergenwuchs |
| Monoamino-dicarbonsäure | Asparaginsäure |
15 |
Asp/D | |
| dito | Asparagin |
16 |
Asn/B | |
| dito | Glutaminsäure |
17 |
Glu/E | Das Mononatriumsalz steigert die geistige Leistungsfähigkeit. In der Lebensmittelindustrie verschiedenen Extrakten zur Geschmackssteigerung zugesetzt |
| dito | Glutamin |
18 |
Gln/Q | |
| Heterocyclische Aminosäuren | Prolin |
19 |
Pro/P | |
| dito | Hydroxyprolin |
20 |
||
| dito | Tryptophan* |
21 |
Trp/W | Für die Bildung des Augenpigments. Fehlen bedingt Haarausfall. Star |
| dito | Histidin* |
22 |
His/H | Für die Bildung des Blutfarbstoffs sowie verschiedener Nucleinsäuren. Fehlen bedingt Anämie |
1) Bei dem Code gibt es zwei verschiedene Systeme, das ältere Symbol mit drei Buchstaben und das neuere mit einem Buchstaben.
* Diese Aminosäuren sind für den Menschen essentiell, können also von ihm nicht synthetisiert werden und müssen deshalb dem Körper mit der Nahrung zugeführt werden.
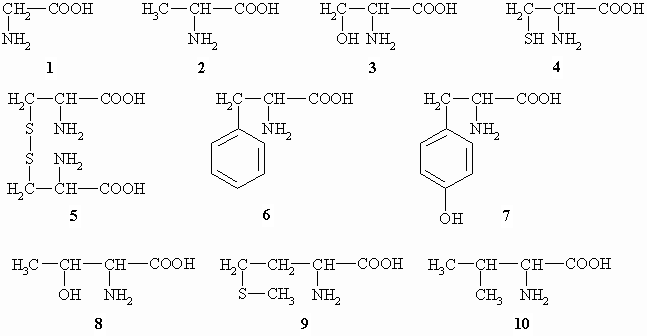
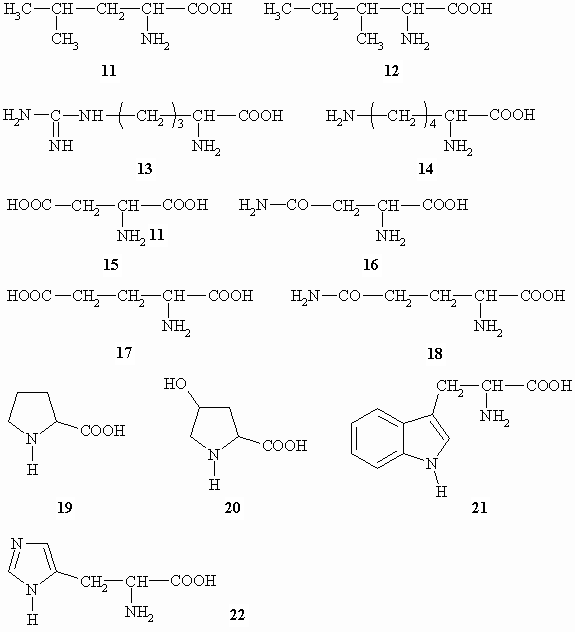
Die folgende Tabelle stellt noch einige seltenere Aminosäuren sowie wichtige Derivate der Aminosäuren vor:
| Name | Strukturformel | Herkunft | Funktion |
| ß-Alanin | H2N-CH2-CH2-COOH | Pantothensäure | |
| a -Amino-buttersäure | CH3-CH2-CH(NH2)-COOH | Corynebacterium diphtheriae | |
| g -Amino-buttersäure | H2N-CH2-CH2-CH2-COOH | Bakterien, Hefe, Pflanzen | Transmitter im Gehirn |
| a ,e -Diamino-pimelinsäure | HOOC-CH(NH2)-(CH2)3-CH(NH2)-COOH | Corynebacterium diphtheriae | |
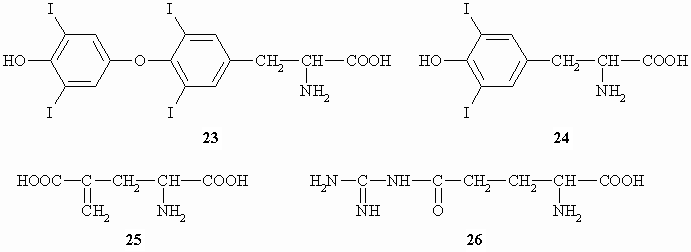
| Thyroxin | Struktur 23, s.o. | Thyreoglobulin | Hormon d. Schilddrüse |
| Diiodtyrosin | Struktur 24, s.o. | Thyreoglobulin | |
| ß-Thiovalin | (CH3)2C(SH)-CH(NH2)-COOH | Penicillin | |
| Lanthionin | S[CH2-CH(NH2)-COOH]2 | Subtilin | |
| Djenkolsäure | CH2[S-CH2-CH(NH2)-COOH]2 | Djenkelnüsse | |
| g -Methylen-glutaminsäure | Struktur 25, s.o. | Erdnuß | |
| a ,g -Diamino-buttersäure | H2N-CH2-CH2-CH(NH2)-COOH | Polymyxine | |
| Ornithin | H2N-CH2-CH2-CH2-CH(NH2)-COOH | Polypeptide | Harnstoff-cyclus |
| Hydroxylysin | H2N-CH2-CH(OH)-(CH2)2– CH(NH2)-COOH | Kollagen | |
| Citrullin | H2N-CO-NH-(CH2)3-CH(NH2)-COOH | Wassermelone, Cassein | Harnstoff-cyclus |
| Canavanin | Struktur 26, s.o. | Sojabohne |
Essentielle Aminosäuren
Wie schon oben erwähnt, kann der menschliche Körper nicht alle Aminosäuren synthetisieren. Nachfolgende Tabelle zeigt den täglichen Mindestbedarf in mg/kg Körpermasse.
|
Aminosäure |
Kind |
Mann |
Frau |
|
Isoleucin |
126 |
450 |
700 |
|
Leucin |
150 |
620 |
1.100 |
|
Lysin |
103 |
500 |
800 |
|
Methionin |
45 |
550 |
1.010 |
|
Phenylalanin |
90 |
1.120 |
1.400 |
|
Threonin |
87 |
300 |
500 |
|
Tryptophan |
22 |
160 |
250 |
|
Valin |
105 |
650 |
800 |
Eigenschaften von Aminosäuren
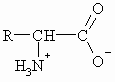
Aminosäuren enthalten eine basische (NH2) und eine saure (COOH) Gruppe im selben Molekül. Sie liegen deshalb zwitterionisch vor. Man nennt dies die Betainstruktur.
Die zwitterionische Struktur der Aminosäuren kann durch ihr elektrophoretisches Verhalten nachgewiesen werden. Bei einem gewissen pH-Wert, dem isoelektrischen Punkt, wandern die Aminosäuren unter der Wirkung einer angelegten Spannung nicht.
Durch Zugabe von Säure wird aus dem nach außen neutralen Zwitterion ein Kation gebildet, das bei der Elektrophorese zur Kathode wandert, während durch Zugabe von Base der Ammoniumcharakter aufgehoben wird und das entstehende Anion zur Anode wandert. Nachfolgend ist die Titrationskurve von Glycin mit der zugehörigen Reaktionsgleichung abgebildet.
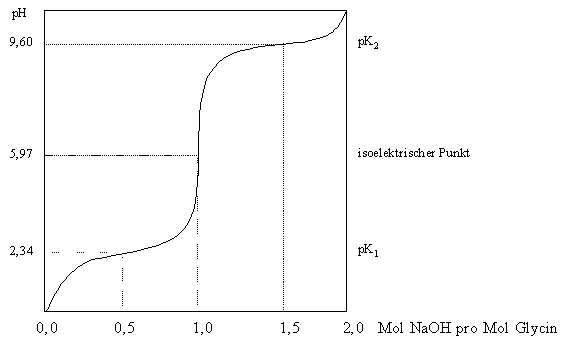
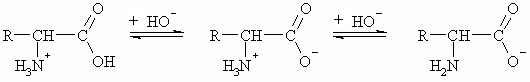
Der pH-Wert des Zwitterions (= isoelektrischer Punkt) ist von der Struktur der Aminosäure abhängig und stellt eine charakteristische Größe dar. Glycin hat den isoelkrtischen Punkt bei pH 5,97.
Wie schon erwähnt, sind außer Glycin alle Aminosäuren optisch aktiv. Sie kommen natürlich überwiegend in der L-Form vor, wie z.B. Alanin:
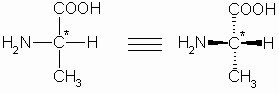
Darstellung von Aminosäuren
Die Darstellung von Aminosäuren kann durch Umsetzung von Halogencarbonsäuren mit Ammoniak durch eine nucleophile Substitution erfolgen. Nach diesem Verfahren sind sowohl α- als auch β- und γ-Aminosäuren zugänglich.
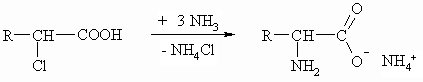
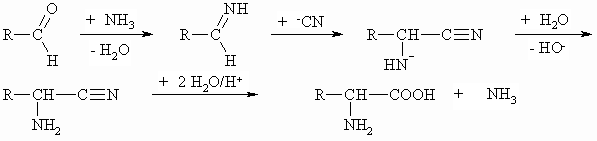
α-Aminosäuren können auch nach der sogenannten Strecker-Synthese dargestellt werden. Hierbei geht man von einem Aldehyd aus, der ein Kohlenstoffatom weniger als die herzustellende Aminosäure hat, und setzt diesen mit Ammoniak und Cyanid um.
Eine weitere Synthese geht, wie der biochemische Weg (Transaminierung), von Ketocarbonsäuren aus. Mit Ammoniak wird zuerst die entsprechende Schiff’sche Base hergestellt, die anschließend zum Amin reduziert wird.
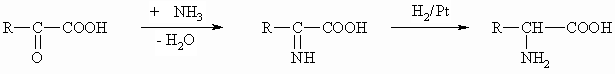
Reaktionen von Aminosäuren
Aminosäuren reagieren wie Amine und Carbonsäuren. So bilden sie z.B. Carbonsäure-Derivate. Hier sind vor allem die Amide zu erwähnen. Zwei oder mehrere Aminosäuren können sich unter Wasserabspaltung zu Amiden verbinden. Dabei entstehen Peptide und Proteine.
Aminosäuren können wie primäre, aliphatische Amine durch ihre Reaktion mit salpetriger Säure nachgewiesen werden. Diese Methode kann man durch gasvolumetrische Messung des entstehenden Stickstoffs quantitativ auswerten (van Slyke).
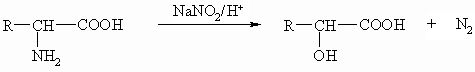
Weiterhin dient der sehr empfindliche Ninhydrin-Test dem Nachweis von Aminosäuren, mit dem noch 0,1 mMol durch ihre intensive Farbreaktion zu erkennen sind.