Nomenklatur der Hydroxycarbonsäuren
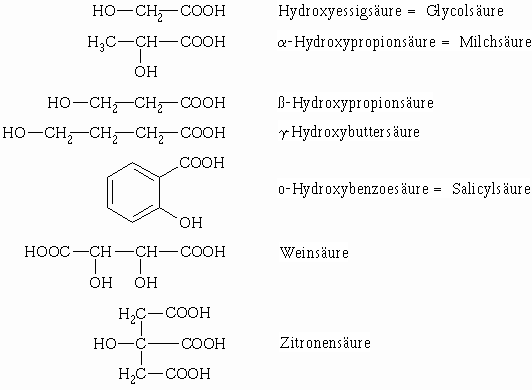
Darstellung von Hydroxycarbonsäuren
Die Hydroxycarbonsäuren können aus den entsprechenden Halogencarbonsäuren durch eine nucleophile Substitutionsreaktion mit Natronlauge dargestellt werden.
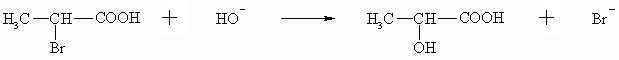
Ein weiteres Verfahren zur Darstellung von a -Hydroxycarbonsäuren beruht auf der Verseifung von Cyanhydrinen (vgl. Kapitel XX). Die Cyanhydrine lassen sich durch Addition von Cyanid an Aldehyde darstellen.
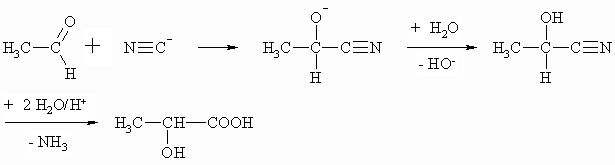
Die Milchsäure, die in den beiden obigen Beispielen hergestellt wird, spielt eine wichtige Rolle im Kohlenhydrat-Abbau des Organismus.
Reaktionen von Hydroxycarbonsäuren
α -, ß-, γ – und δ -Hydroxycarbonsäuren zeigen beim Erhitzen unterschiedliches Verhalten. α -Hydroxycarbonsäuren, wie die Milchsäure, liefern dabei intermolekulare, cyclische Doppelester, die Lactide genannt werden.
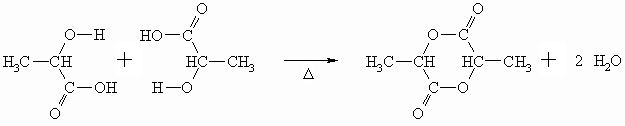
ß-Hydroxycarbonsäuren spalten dagegen intramolekular Wasser unter Bildung einer α- ,ß-ungesättigten Carbonsäure, ab. Es entsteht dabei ein durch Mesomerie stabilisiertes, konjugiertes System.
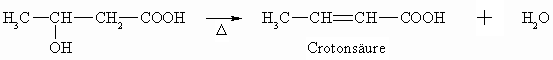
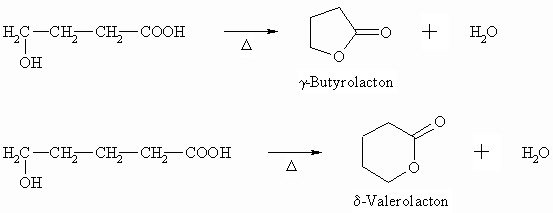
γ – und δ -Hydroxycarbonsäuren spalten ebenfalls intramolekular Wasser ab. Hierbei entstehen jedoch cyclische Ester, die Lactone genannt werden.
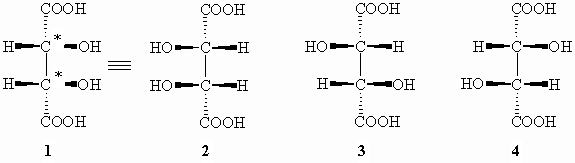
Stereoisomere der Weinsäure
Die Weinsäure besitzt zwei Asymmetriezentren (*). Beide können zu einer Links- oder Rechtsdrehung der Ebene des polarisierten Lichts führen. Im allgemeinen kann eine Verbindung mit n Asymmetriezentren 2n Isomere haben. Das wären hier vier Isomere. Aus Gründen der Symmetrie im Molekül sind bei der Weinsäure die folgenden Strukturen 1 und 2 jedoch identisch; das Molekül darf in der Papierebene um 180° gedreht werden. Die beiden Asymmetriezentren drehen die Ebene des polarisierten Lichts um den gleichen Betrag aber mit unterschiedlichem Vorzeichen. Dadurch wird der Drehsinn intramolekular kompensiert und die Verbindung ist optisch inaktiv. Man nennt diese Verbindung Mesoweinsäure (1 = 2). Die beiden Strukturen 3 und 4 verhalten sich wie Bild zu Spiegelbild und werden als D-Weinsäure (3) und L-Weinsäure (4) benannt. Es handelt sich hierbei also um Enantiomere. Die Mesoweinsäure nimmt konfigurativ in Bezug auf die beiden optisch aktiven Weinsäuren eine Sonderstellung ein. Sie ist kein Spiegelbildisomeres zur D- und L-Weinsäure, sondern steht zu diesen im Verhältnis der Diastereomerie. Die Diastereomerie tritt nur bei Verbindungen mit zwei oder mehreren Asymmetriezentren auf. Sie liegt dann vor, wenn nur ein Teil der Asymmetriezentren gespiegelt sind und die restlichen übereinstimmen. In Diastereomeren sind die Abstände der Atomgruppen im Molekül verschieden; sie besitzen daher unterschiedliche chemische und physikalische Eigenschaften.
Das Gemisch aus gleichen Teilen von D- und L-Weinsäure, also das Razemat, wird auch als Traubensäure bezeichnet.
Zitronensäure
Unter den Hydroxytricarbonsäuren besitzt die Zitronensäure biologische Bedeutung. Sie entsteht beim Abbau der Kohlenhydrate. Diese Verbindung besitzt kein Asymmetriezentrum, ist also nicht optisch aktiv.